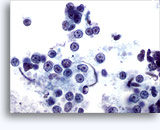
Fijnenaald Aspiratie Cytologie
Overige lichaamsdelen
Michele M. Weir, MD, FRCP
Inleiding
Dit hoofdstuk gaat over de fijne naald aspiratie biopsieën (FNAB) van de nieren, bijnieren, gonaden, botten en zacht weefsel.
FNAB van de nieren
FNAB van een renale massa is een ongebruikelijke procedure, omdat de meeste patiënten met een renale massa direct geopereerd worden. FNAB speelt echter wel een rol bij de beoordeling van een renale massa als:
- de kenmerken op de foto onbepalend zijn voor classificatie;
- de patiënt geen operatiekandidaat is; en
- operatieplanning vereist is (nier- of uterusbesparende operatie)
Van FNAB van renale tumoren wordt gerapporteerd dat deze een gevoeligheid heeft van 79-92%, een specificiteit van 92-99% en een algehele diagnostische nauwkeurigheid van 73-95%. Door tumorheterogeniteit en het belang van cytogenische classificatie, wordt de definitieve diagnose van sommige renale neoplasma’s het best gesteld op basis van histologische monsters. Bepaalde oncocytische neoplasma’s die negatief zijn voor de Hale colloïdaal ijzerkleuring, zijn soms moeilijk verder te subtyperen op basis van FNAB. Daarom zou alleen een differentiële diagnose gesteld moeten worden.
Bij volwassenen is de meest voorkomende niet-neoplastische oorzaak van een renale massa een niercyste. Andere laesies kunnen veroorzaakt worden door abcessen en xantogranulomatose pyelonephritis. Onder de renale neoplasma’s wordt de meest voorkomende benigne entiteit gevormd door oncocytomen en de meest voorkomende maligne entiteit door renaal celcarcinomen (RCC). Overige neoplasma’s zijn onder andere benigne angiomyolipoom en nierbekken utotheelcarcinoom.
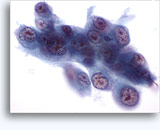
Cytologie van FNAB van de nieren
- Normaal
- Monsters hebben lage celrijkdom
- Geïsoleerde cellen, of kleine groepen
- Glomeruli:
- capillaire lussen, spoel- en ronde cellen
- geen atypie, geen bolletjes of papillen (in tegenstelling tot papillair RCC)
- cellulaire globulaire structuren
- nagebootst door: papillaire RCC
- Proximaal gekronkeld nierkanaal:
- tubules en lagen
- overvloedig granulair cytoplasma
- slecht gedefinieerd fragiel cytoplasma zonder celgrenzen (in tegenstelling tot oncocytoom)
- ongedetailleerde kern, prominente nucleolus
- nagebootst door: oncocytoom, RCC
- Distaal gekronkeld nierkanaal/verzamelkanaal (DCT/CD):
- tubules, platte lagen (in tegenstelling tot RCC)
- goed gedefinieerd cytoplasma, kleinere cellen
- geen vacuolen (in tegenstelling tot RCC)
- geen nucleolus
- nagebootst door: RCC
- Oncocytoom
- Schone achtergrond
- Onsamenhangende losse cellen of losse clusters, geen naakte kernen
- Zelden in grote groepen(in tegenstelling tot RCC)
- Kleine uniforme kernen, gladde grenzen (in tegenstelling tot RCC)
- Focale nucleaire atypie, tweekernigheid, onopvallende nucleoli
- Overvloedig uniform granulair goed afgebakend cytoplasma
- Geen vacuolen (in tegenstelling tot RCC)
- Scherpe, goed afgebakende celgrenzen (in tegenstelling tot PCT cellen)
- Vimentin negatief, cytokeratine 8/18 positief (gebruik biotineblok)
- Negatief voor Hale’s colloïdale ijzerkleuring, of perinucleaire/atypische kleuring aanwezig
- Elektronenmicroscopie: Mitochondria
- NAGEBOOTST DOOR: PCT, chromofobe RCC, conventionele RCC met granulair cytoplasma
- Niercelcarcinoom
- Conventioneel/algemeen/helder celtype (CRCC)
- heldere of necrotische achtergrond
- Cohesieve eenlagige lagen(in tegenstelling tot oncocytoom)
- prominent vertakkende haarvaten
- zeldzame losse cellen (laaggradig) –> meer losse cellen en naakte kernen (meer hooggradig) (in tegenstelling tot oncocytoom)
- ongedetailleerde kernen, geen nucleoli (laaggradig)
- grotere atypische kernen, enkele vreemde, nucleoli prominent (hogergradig), (in tegenstelling tot oncocytoom, chromofobe RCC)
- excentrische kern, uit cel gedreven
- meer uniforme kernen dan chromofobe RCC
- schuimachtig gevacuoliseerd cytoplasma (in tegenstelling tot ONC en normaal)
- Helder, of granulair (niet uniform) overvloedig cytoplasma (laag N/C-ratio)
- intracytoplasmische Mallory-achtige lichamen
- vimentin, cytokeratine positief (gebruik biotineblok)
- Hale colloïdaal ijzer negatief
- Elektronenmicroscopie: glycogeen, lipide, soms mitochondria
- NAGEBOOTST DOOR: distaal gekronkeld nierkanaal en verzamelkanaal, oncocytoom, chromofobe RCC
- Chromofobe type
- schone achtergrond
- lagen, clusters, losse cellen (onsamenhangend, maar minder dan CRCC)
- naakte kernen (in tegenstelling tot oncocytoom)
- meer variatie in cel, kerngrootte (dan oncocytoom, CRCC)
- vesiculaire kernen, tweekernigheid, inclusies
- onregelmatige nucleaire omtrek (in tegenstelling tot oncocytoom, CRCC)
- prominente nucleoli in enkele
- overvloedig granulair cytoplasma
- perinucleaire clearing, prominente clegrenzen (“koilocyten”)
- donzig/helder/granulair niet uniform cytoplasma
- vimentin negatief, cytokeratine positief (gebruik biotineblok)
- Hale colloïdaal ijzer positief – uniform, dens, cytoplasmisch
- elektronenmicroscopie: microblaasjes, mitochondria in geval van eosinofiele variant
- NAGEBOOTST DOOR: oncocytoom, CRCC
- Conventioneel/algemeen/helder celtype (CRCC)
FNAB van bijnieren
FNAB van een bijniermassa wordt doorgaans uitgevoerd om een metastase te bevestigen, of voor de afhandeling van een incidentele knobbel. Een functioneel of verdacht pheochromocytoom is een contra-indicatie voor FNAB, door de mogelijke hypertensieve crisis en/of overlijden. Voor FNAB van bijniertumoren wordt een gevoeligheid gemeld van 85-94% en voor metastasen een specificiteit van 100%.
Bij volwassenen is het meest voorkomende neoplasma in de bijnieren een metastase van de long of borst. Andere veel voorkomende bronnen zijn het gastro-intestinale kanaal, nier en huid (melanoom) Primaire bijnierneoplasma’s kunnen onder andere van corticale oorsprong (adenoom, carcinoom) of van medullaire oorsprong (pheochromocytoom) zijn. Andere primaire bijnierlaesies omvatten myelolipoom, cysten en corticale Nudulaire hyperplasie.
Cytologie van FNAB van bijnieren
- Normaal
- Lage celrijkdom
- Schors: buitenste lagen
- schuimachtige lipiderijke achtergrond
- losse cellen, clusters
- ongedetailleerde ovale kernen
- geen of kleine nucleoli
- overvloedig gevacuoliseerd cytoplasma met rafelige randen
- NAGEBOOTST DOOR: is soms niet te onderscheiden van benigne corticale nodule, sommige corticale bijniercarcinomen
- Schors: Binnenste laag
- geen vacuolatie
- granulair eosinofiel cytoplasma
- kleinere cellen
- ouderdomspigment
- Medulla:
- basofiel cytoplasma
- grote excentrische kern
- verdachte nucleoli
- fijnkorrelige chromatine
- Benigne nodule in de niercortex
- Kan celmonster zijn
- Schuimachtige lipiderijke achtergrond (afwezig in RCC)
- Cohesieve fragmenten met sinusoidale endotheelcellen
- Naakte kernen
- Ronde tot ovale kernen (meer uniform) dan RCC)
- Geen of kleine nucleolus
- Multinucleatie
- Gevacuoliseerd cytoplasma (meer dan RCC)
- Vimentin positief, cytokeratine (laag moleculair gewicht), positief in enkele gevallen
- Inhibin, Melan-A, calretinine positief
- EMA, CK7, CK20 Negatief
- NAGEBOOTST DOOR: RCC en is soms niet te onderscheiden van normale bijnier en sommige corticale bijniercarcinomen.
- Corticaal bijniercarcinoom
- Bootst eigenschappen adenoom na
- Er kan necrose aanwezig zijn
- Er kunnen maligne kerncriteria waargenomen worden
- Histologische beoordeling vereist om grotere adenomen van carcinomen te onderscheiden
- Gelijk immuunprofiel als adenoom
- NAGEBOOTST DOOR: Is soms niet te onderscheiden van normale bijnier en corticaal bijnieradenoom, pheochromocytoom, andere maligniteiten, indien slecht gedifferentieerd.
- Feochromocytoom
- 3 celtypes
- nr. 1 – fibrillair cytoplasma, ovale hyperchromatische kernen, kunnen anisonucleose/pleomorfisme/binucleatie vertonen
- spoelcellen (sustenaculaire cellen)
- plasmacytoïde cellen
- Melaninepigment in enkele
- Dyshesieve losse cellen, enkele clusters
- Prominente variatie in kerngrootte en vorm
- Rode cytoplasmische granulariteit bij luchtgedroogd materiaal
- Synaptophysine, chromogranin positief; S-100 Posititief in spoelcellen
- NAGEBOOTST DOOR: Corticaal bijniercarcinoom, andere slecht gedifferentieerde maligniteiten
- 3 celtypes
- Metastatisch carcinoom
- Uniforme celpopulatie
- Maligne kerncriteria, kunnen neuroendocriene kenmerken hebben
- Glandulaire of squameuze differentiatie van het cytoplasma kan aanwezig zijn
- Er kan necrose aanwezig zijn
- Cytokeratine positief
- CK7, CK20-profiel kan plaats van oorsprong verduidelijken
- Doorgaans Inhibin, Melan-A, calretinine negatief
- TTF-1 kan helpen bij confirmatie longoorsprong
- NAGEBOOTST DOOR: Pheochromocytoom, corticaal bijniercarcinoom, andere slecht gedifferentieerde maligniteiten
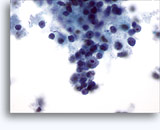
Afbeeldingen 22-23:Kleine cellen met hyperchromatische en vlekkerige kernen met molding, weinig cytoplasma en hoge N/C-ratio’s. Achtergrond bevat necrotisch granulair materiaal.
FNAB van ovarium en testis
FNAB van ovarium en testus wordt heel zelden gebruikt voor de primaire diagnose van gonadale neoplasma’s. In Noord-Amerika speelt FNAB een rol bij de diagnose van terugkerende of metastatische gonadale maligniteiten. Bij deze toepassing wordt voor de diagnostische gevoeligheid van FNAB een waarde gemeld die varieert van 65-95%, en een hogere specificiteit (92-100%). Redenen voor een vals negatieve uitslag zijn onder andere bemonsteringsfouten ten gevolge van door bestraling geïnduceerde fibrose, de omvang van de massa, of de aanwezigheid van necrose, en interpretatiefouten (misinterpretatie als benigne).
Geselecteerde cytologie van FNAB van het ovarium
- Sereus adenocarcinoom
- Cellulaire monsters
- Papillen, sommige vertakt
- Enkele losse cellen
- Maligne kerncriteria, maar deze kunnen afwezig zijn indien laaggradig
- Intracytoplasmische vacuolen
- Psammomalichamen naakt, of in celgroepen (niet-specifieke bevinding)
- NAGEBOOTST DOOR: andere carcinomen (primair en secundair) indien laaggradig, niet te onderscheiden van sereuze borderline tumor
Geselecteerde cytologie van FNAB van de testis
- Seminoom
- Verspreide grote cellen en weinig clusters
- Naakte kernen, delicaat cytoplasma
- Primitieve cellen: Centrale kernen, fijn vesiculair chromatine, prominente centrale nucleolus
- Achtergrondlymfocyten, epithelioïde histiocyten
- Tigroïde achtergrond (schuimig, streepachtig, kan afwezig zijn of minimaal in dunne laag preparaten)
- PLAP positief, LCA, AFP, cytokeratine negatief
- NAGEBOOTST DOOR: Andere kiemceltumoren, maligne lymfoom
- Embryonaal carcinoom
- Necrose aanwezig
- Papillair, klierachtig, of in lagen
- Pleomorfe kernen, grof chromatine, verscheidene prominente nucleoli
- PLAP cytokeratine positief; AFP kan positief zijn, LCA negatief
- NAGEBOOTST DOOR: andere kiemceltumoren, maligne lymfoom, melanoom, hooggradig carcinoom
FNAB van bot en zacht weefsel
FNAB van bot en laesies van zacht weefsel wordt doorgaans uitgevoerd op een metastatische ziekte te bevestigen, meestal een carcinoom. In sommige centra kan FNAB gebruikt worden voor de diagnose van geselecteerde primair bot en zacht weefsel sarcomen. Diagnostische nauwkeurigheid is het hoogst voor FNAB van metastatische neoplasma’s (bereik van 92-100%).
Cytologie FNAB van metastasen van bot en zacht weefsel
- Metastatisch carcinoom
- Soms necrose
- Maligne nucleaire eigenschappen
- Clusters van cellen en losse cellen (dishesie)
- Neuroendocriene differentiatie: hoge N/C-ratio’s, vlekkerige hyperchromatische kernen met molding en weinig cytoplasma
- Glandulaire differentiatie: intracytoplasmische vacuolen, celballen, papillen, klieren
- Squameuze differentiatie: keratinisatie, hard refractiel cytoplasma
- Urotheliale differentiatie: cercariforme cellen (cytoplasmische uitlopers)
- Cytokeratine doorgaans positief
- Metastatisch maligne melanoom
- Dishesieve losse cellen
- Maligne nucleaire eigenschappen, excentrische kernen
- Reeks van patronen: Klein, spoel- of epithelioïde cellen
- Variatie in nucleaire grootte
- Nucleaire pseudoinclusies met bi- en multinucleatie
- Intracytoplasmisch stoffig bruin melanine pigment
- S-100, HMB-45, Melan-A positief (niet altijd)
- Maligne lymfoom
- Dishesieve losse cellen
- Open granulair chromatine
- Nucleoli gebaseerd op kernmembraan in sommige subtypes
- Uitsteeksels van celkernmembraan en onregelmatigheid
- Weinig cytoplasma in sommige subtypes (hoge N/C-ratio’s)
- Lymfoglandulaire lichamen op de achtergrond
- LCA positief, B of T celafstamming
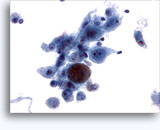
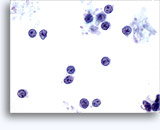
Afbeeldingen 37-38: Dishesieve losse cellen met hogeN/C-ratio’s, weinig cytoplasma, open chromatine, kernuitsteeksels en nucleoli in membraan. Lymfoglandulaire lichamen op de achtergrond.
Referenties
- Bommer KK, Ramzy I and Mody D. Fine-Needle Aspiration Biopsy in the Diagnosis and Management of Bone Lesions. Cancer (Cancer Cytopathology) 1997; 81:148-56.
- Caraway NP, Fanning CV, Amato RJ and Sneige N. Fine-Needle Aspiration Cytology of Seminoma: A Review of 16 Cases. Diagnostic Cytopathology 1995; 12:327-33.
- Geisinger KR et al. Modern Cytopathology. Philadelphia, Churchill Livingstone. 2004; pp 579-606, 689-700.
- Kabukcuoglu F, Kabukcuoglu Y, Kuzgun U and Evren I. Fine Needle aspiration of Malignant Bone Lesions. Acta Cytologica 1998;42:875-82.
- Liu J, Fanning CV. Can Renal Oncocytomas be Distinguished from Renal Cell Carcinoma on Fine-Needle Aspiration Specimens? Cancer (Cancer Cytopathol) 2001;93:390-7.
- Nguyen G and Akin MM. Fine Needle Aspiration Cytology of the Kidney, Renal Pelvis and Adrenal. In:Clinics in Laboratory Medicine. Stanley MW editor. Philadelphia. WB Saunders Company. 1998;18(3):429-60.
- Renshaw AA, Granter SR, Cibas ES. Fine-Needle Aspiration of the Adult Kidney. Cancer (Cancer Cytopathol) 1997;81:71-88.
- Renshaw, AA, Lee KR, Madge R, Granter SR. Accuracy of Fine Needle Aspiration in Distinguishing Subtypes of Renal Cell Carcinoma. Acta Cytol 1997;41:987-94.
- Wakely PE, Kneisl, JS. Soft Tissue Aspiration Cytopathology. Cancer (Cancer Cytopathol) 2000;90:292-8.
- Wiatrowska, BA, Zakowski MF. Fine-Needle Aspiration Biopsy of Chromophobe Renal Cell Carcinoma and Oncocytoma. Cancer (Cancer Cytopathol) 1999;87:161-7.
- Wu H H, Cramer HM, Kho J and Elsheikh, TM. Fine Needle Aspiration Cytology of Benign Adrenal Cortical Nodules. Acta Cytologica 1998;42:1352-8.
- Yang B, Syed ZA and Rosenthal DL. CD10 Facilitates the Diagnosis of Metastatic Renal Cell Carcinoma From Primary Adrenal Cortical Neoplasm in Adrenal Fine-Needle Aspiration. Diagn. Cytopathol. 2002;27:149-52.
- Zardauin IM. Renal FNAC Acta Cytol 1999;43:184-90.
- Zhang, PJ, Genega EM, Tomaszewski JE, Pasha TL, LiVolsi VA. The Role of Calretinin, Inhibin, Melan-A, BCL-2, and C-kit in Differentiating Adrenal Cortical and Medullary Tumors: An Immunohistochemical Study. Mod Pathol 2003;16(6):591-7.