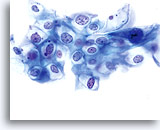
LÉSION MALPIGHIENNE INTRA-ÉPITHÉLIALE DE BAS GRADE (LSIL)
LÉSION MALPIGHIENNE INTRA-ÉPITHÉLIALE DE BAS GRADE (LSIL)
Diane D. Davey, MD
La dysplasie malpighienne se caractérise par la présence d’au minimum certaines caractéristiques malpighiennes dans le cytoplasme des cellules anormales. (Suggestions de lectures 1) Le grade de la dysplasie reflète la maturité des cellules impliquées. Par exemple, dans la dysplasie légère, les cellules ressemblent à des cellules superficielles et intermédiaires métaplasiques matures, tandis qu’un épithélium plus gravement dysplasique reflète un état normal moins mature comme des cellules parabasales et/ou immatures de type métaplasique. Avec l’émergence du “système Bethesda de classification des diagnostics cervico-vaginaux”, l’utilisation du terme “dysplasie” a diminué en faveur du terme lésions malpighiennes intra-épithéliales de bas grade (LSIL) ou lésions malpighiennes intra-épithéliales de haut grade (HSIL). Dans cet atlas, nous utiliserons la terminologie du système Bethesda.
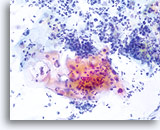
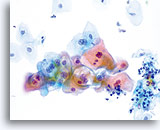
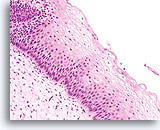
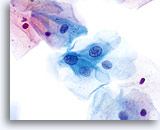
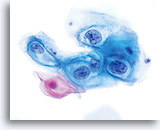
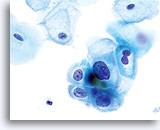
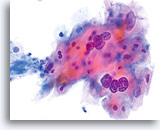
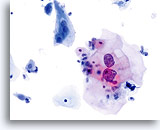
La morphologie des LSIL (y compris des changements associés au virus du papillome humain, HPV) est essentiellement identique sur les lames ThinPrep et les frottis conventionnels. Cette similitude est en partie due à la capacité de la cellule malpighienne mature à conserver son intégrité malgré la fixation inadéquate ou l’artefact d’étalement inhérents aux frottis conventionnels. Cette intégrité résulte de la rigidité cellulaire due à la kératinisation cytoplasmique.
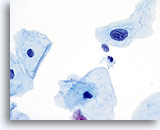
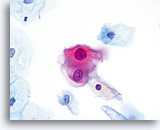
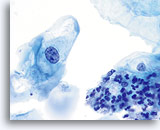
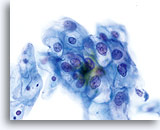
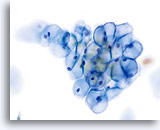
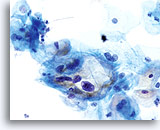
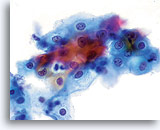
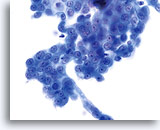
En raison de leur morphologie, les cellules issues de lésions de bas grade comptent parmi les anomalies intra-épithéliales les plus faciles à localiser et à identifier. En comparaison, les noyaux LSIL sont les plus grands et présentent un rapport N/C inférieur aux HSIL ou carcinomes. Ces cellules affichent une atypie nucléaire plus importante que les ASCUS (ce qui se traduit par une augmentation de la taille nucléaire, une irrégularité de la chromatine et une irrégularité de l’enveloppe nucléaire). Les noyaux peuvent occasionnellement ne pas être aussi hyperchromatiques que sur les frottis conventionnels, mais ils le sont toujours par rapport aux cellules normales environnantes. Les changements associés au HPV (par exemple, formation de cavités dans le cytoplasme) sont plus évidents grâce à la fixation liquide et à la technique de transfert, ce qui élimine la déformation des cellules associée à la méthode d’étalement conventionnelle. La méthode ThinPrep préserve mieux ces changements cellulaires, ce qui permet une meilleure distinction entre les véritables cavités cytoplasmiques induites par le HPV et les vacuoles bénignes/dégénératives et/ou les cellules malpighiennes glycogénées.
Comme il s’agit de cellules malpighiennes matures, elles gardent leur forme polygonale et conservent en partie leur taille normale. La taille des noyaux est au moins 3 à 4 fois supérieure à celle d’une cellule intermédiaire normale. En revanche, quand les changements associés au HPV sont évidents, les cellules peuvent être plus petites (quasiment parakératosiques), tout comme les noyaux (quelque peu pycnotiques) qui présentent en outre une binucléation et/ou multinucléation. Ces noyaux pycnotiques affichent en outre des caractéristiques anormales : hyperchromasie, augmentation de la taille par rapport à une cellule malpighienne superficielle normale, légère variation de la forme et de la taille, etc. Il est important d’insister sur le fait qu’une interprétation de LSIL/HPV implique des cavités cytoplasmiques nettes accompagnées de la morphologie nucléaire anormale décrite ci-dessus.
Dans certains cas, on trouve un mélange de cellules LSIL et HSIL, et l’anomalie la plus grave doit être interprétée en priorité sur la lame ThinPrep. Il s’avère parfois difficile de faire la distinction entre les LSIL et les HSIL. Les critères en faveur des HSIL incluent un rapport N/C élevé, un cytoplasme immature et un nombre plus important d’anomalies nucléaires. En raison du manque de cellules anormales ou de critères véritablement intermédiaires, les cas rares de SIL ne peuvent pas être placés dans une catégorie. Comme ces cas vont probablement progresser, il semble plus prudent d’utiliser un terme tel que “SIL, grade impossible à déterminer”. Même si la plupart des études de suivi des LSIL TP font le plus souvent apparaître des changements de bas grade associés à la biopsie, environ 15 à 20 % des cas de LSIL sont suivis de biopsies de haut grade.
ENTITÉS SEMBLABLES (Diagnostics différentiels) :
Sans grande surprise, la lésion LSIL possède peu d’entités semblables, même si elles sont plus faciles à différencier grâce à la fixation immédiate de la méthode ThinPrep®, ce qui permet une meilleure visualisation des cellules et de leurs caractéristiques. Pour connaître les critères différentiels et voir des images de LSIL classées ASCUS, voir le chapitre consacré à la catégorie ASCUS.
| RÉACTION (Organisme ou inflammation) |
RÉPARATION (Type) |
LSIL (HPV) |
|
| Présentation cellulaire | Isolées ou en groupes | Amas et groupes plats | Isolées ou en groupes |
| Type de cellules | Tous les types | Cellules endocervicales/métaplasiques | Cellules malpighiennes matures |
| Noyaux | Taille augmentée jusqu’à 1,5 fois
Binucléation/ multinucléation éventuellement présente Membranes nucléaires lisses |
Augmentation de taille variable – légère à marquée
Binucléation/ multinucléation éventuellement présente Membranes nucléaires lisses |
Taille augmentée 3 à 4 fois
Binucléation/ multinucléation éventuellement présente avec HPV Membranes nucléaires lisses à légèrement irrégulières |
| Chromatine | Finement granulaire, répartie de façon homogène
Hyperchromasie non évidente |
Finement granulaire, répartie de façon homogène
Hyperchromasie non évidente |
Finement à grossièrement granulaire, répartie de façon homogène
Légèrement hyperchromatique |
| Nucléoles | Petits et souvent multiples, uniformes | Petits à bien visibles, souvent multiples | Discrets ou absents |
| Présentation cytoplasmique | Halos périnucléaires souvent présents, petits, plusieurs vacuoles peuvent être évidentes en raison de la dégénérescence | Cytoplasme vacuolisé avec présentation de culture tissulaire lâche | Dense, forme polygonale avec ou sans cavité nette et bien définie associée au HPV, bord périphérique dense du cytoplasme |
- Austin RM: Follow-up of Abnormal Gynecologic Cytology. A College of American Patholgists Q-Probes Study of 16,312 Cases from 306 Laboratories. Arch Pathol Lab Med 2000;124(8):1113-4
- Carpenter AB, Davey D: ThinPrep Pap Test: performance and biopsy follow-up in a university hospital. Cancer 1999;41:39-44.
- DeMay RM: The Art and Science of Cytopathology. Chicago: ASCP Press; 1996
- Diaz-Rosario LA et al: Performance of a fluid-based, thin-layer Papanicolaou smear method in the clinical setting of an independent laboratory and an outpatient screening population in New England. Arch Pathol Lab Med 1999; Sep 123(9):817-21.
- Grace, A, et al: Comparative study: Conventional cervical and ThinPrep Pap Tests in a routine clinical setting. Cytopathol 2002;13:200-05.
- Guidos BJ, Selvaggi SM: Use of the ThinPrep Pap Test inclinical practice. Diagn Cytopathol 1999;20:70-73.
- Lee KR et al: Comparison of conventional Papanicolaou smears and a fluid-based, thin-layer system for cervical cancer screening. Obstet Gynecol 1997;90:278-284.
- Luthra, UH, et al: Performance of monolayered cervical smears in a gynecology outpatient setting in Kuwait. Acta Cytol 2001; 46(2):303-10.
- Weintraub J, Morabia A: Efficacy of a liquid-based thin layer method for cervical cancer screening in a population with a low incidence of cervical cancer. Diagn Cytopathol 2000 Jan;22(1):52-9.