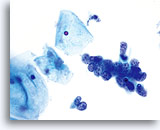
ANOMALIES CELLULAIRES ÉPITHÉLIALES
ANOMALIES CELLULAIRES ÉPITHÉLIALES
ADÉNOCARCINOME ENDOMÉTRIAL
Luis A. Diaz-Rosario, MD
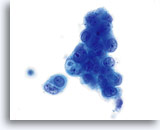
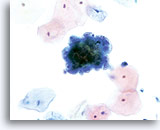
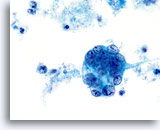
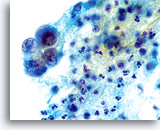
L’adénocarcinome endométrial représente l’affection maligne gynécologique la plus répandue (2/3 des cancers du col de l’utérus). D’un point de vue clinique, il se répartit en deux types. Le type I (qui représente 2/3 des adénocarcinomes endométriaux) touche généralement les femmes pré- ou périménopausées avec antécédents cliniques d’hyperoestrogénie endogène ou exogène. Il évolue généralement vers un processus néoplasique allant de l’hyperplasie à l’adénocarcinome invasive bien différencié. Réagissant habituellement à l’hormonothérapie, son pronostic est meilleur que celui des tumeurs de type II. Le type II (qui représente 1/3 des adénocarcinomes endométriaux) touche généralement les femmes post-ménopausées sans hyperoestrogénie. Il se présente habituellement sous la forme de néoplasmes mal différenciés. Le diagnostic d’adénocarcinome bien ou mal différencié de l’endomètre repose sur l’examen de cellules prélevées dans le col de l’utérus. Que ce soit sur frottis conventionnel ou sur lame ThinPrep®, la présentation cytologique de l’adénocarcinome endométrial dépend largement du grade et du type du néoplasme. Comme les lésions endométriales ne sont pas prélevées directement pour un test de Pap, les néoplasmes de grade supérieur ont tendance à exfolier davantage de cellules et à être plus évidents. La distribution uniforme et la fixation liquide des cellules dans les échantillons ThinPrep peuvent faciliter la détection des lésions bien différenciées, qui présentent généralement un faible nombre de cellules anormales et des changements cellulaires subtils précoces.
Même s’il faut toujours les prendre en compte, les antécédents de la patiente sont extrêmement importants lorsqu’il s’agit d’identifier des cellules endométriales sur le frottis. En effet, l’âge de la patiente et ses antécédents peuvent jouer un rôle important dans le diagnostic de cellules bénignes, atypiques et franchement malignes. Un adénocarcinome endométrial bien différencié peut s’avérer cytologiquement complexe à distinguer d’un endomètre bénin ou d’une hyperplasie endométriale. Des études et publications supplémentaires permettraient par conséquent de mieux définir ces critères.
Dans l’adénocarcinome endometrial, le degré d’atypie augmente avec le grade tumoral. Les cellules peuvent être bénignes à franchement malignes. Dans les critères ci-dessous, nous décrirons les caractéristiques des cellules franchement malignes à utiliser comme base cytologique.
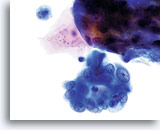
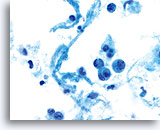
D’un point de vue cytologique, les néoplasmes de type I présentent des cellules endométriales atypiques/malignes sur un fond à l’indice de maturation supérieur. À l’inverse, les néoplasmes de type II se présentent généralement sur un fond atrophique. Sur les lames ThinPrep, les cellules endométriales sont bien conservées et peuvent apparaître dans des groupements 3D encombrés de taille variable et de petits amas plats contenant peu de cellules. Les cellules semblent généralement plus grandes que leurs homologues normales. Les bordures lisses, parfois festonnées, des groupes leur confèrent une configuration papillaire. Le cytoplasme est finement à discrètement vacuolisé. Certaines vacuoles plus grandes compriment le noyau sur un côté de la cellule. On observe parfois une phagocytose des polynucléaires. Les caractéristiques nucléaires dépendent du grade de la tumeur. En général, quand la tumeur devient moins différenciée, le noyau a tendance à se regrouper. On observe en outre une augmentation graduelle de la surface nucléaire (µm²), de la taille et du nombre de nucléoles, des irrégularités dans la répartition et une texture grossière de la chromatine, ainsi qu’un épaississement des membranes nucléaires.
Les critères cytologiques suivants permettent de détecter un adénocarcinome endométrial sur des lames ThinPrep® :
Phagocytose des polynucléaires dans le cytoplasme.
60x
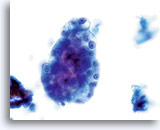
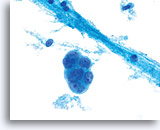
Cellules généralement plus grandes que leurs homologues normales.
60x
Noyaux “regroupés” par rapport à leurs homologues normaux.
60x
Membranes nucléaires épaissies.
60x
Chromatine en motte et répartition non homogène.
60x
Nucléoles courants, de fréquence/taille/nombre variables.
60x
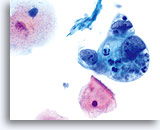
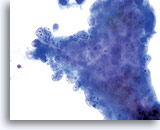
La méthode ThinPrep® permet de conserver les indices contextuels observés dans le fond de ces lésions. La diathèse tumorale, le plus souvent observée sous la forme d’une diathèse séreuse sur les frottis conventionnels, se présente sous forme de débris granulaires en motte sur les lames Thin Prep® (les détails cellulaires sont ainsi nettement visibles).
Diathèse tumorale et cellules malignes isolées.
60x
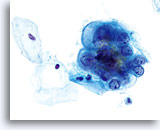
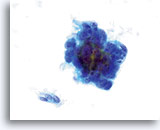
Groupes de cellules d’un adénocarcinome endométrial accompagné de diathèse tumorale.
60x
Entités semblables
L’adénocarcinome endometrial possède peu d’entités semblables, mais l’âge et les antécédents de la patiente peuvent faciliter les diagnostics différentiels. De type spécifiquement endométrioïde, l’adénocarcinome endométrial peut ressembler à l’adénocarcinome endocervical. Il peut se présenter sous forme d’un amas plutôt que sous une forme papillaire globale totale. L’adénocarcinome endométrioïde peut être complexe à distinguer s’il siège principalement dans l’utérus et s’étend dans le col (ou vice versa).
En raison de la petite taille des cellules et de l’absence de cytoplasme, le SCC à petites cellules représente une autre entité semblable potentielle de l’adénocarcinome endométrial.
Note : Les cellules endométriales observées dans l’hyperplasie et l’hyperplasie atypique peuvent être difficiles à différencier d’un néoplasme (voir la section sur la catégorie AGUS).
| Adénocarcinome endométrial | Adénocarcinome endocervical | SCC À PETITES CELLULES | |
| Présentation tissulaire | Petits groupes lâches, billes cellulaires (groupes 3D) et larges amas dans les tumeurs mal différenciées | Quelques cellules isolées, bandes, rosettes et amas/groupes 2D avec bordures bien définies (festonnées) | Cellules isolées et agrégats ou disposition en syncytium. Plate, moins de groupes. |
| Cytoplasme | Finement à discrètement vacuolisé avec certaines vacuoles larges, rapport N/C 2:1 à cytoplasme très peu abondant | Finement vacuolisé avec vacuoles discrètes isolées occasionnelles, rapport N/C 2:1 | Cytoplasme rare et finement vacuolisé ou délicat. |
| Noyau | Légère augmentation à augmentation de la taille (légèrement plus grande que le noyau des cellules intermédiaires), généralement rond à ovale | Augmentation de la taille (3 à 4 fois plus grande que le noyau des cellules intermédiaires), rond à ovale | Généralement rond à ovale et occupant jusqu’à 95 % du cytoplasme. Formes pycnotiques possibles |
| Membrane nucléaire | Lisse, épaissie | Lisse à irrégulière (ondulante), épaissie | Lisse à irrégulière, épaissie |
| Chromatine | Grossière, répartition homogène, élimination de la parachromatine, légère hyperchromasie | Grossière, granulaire et hyperchromatique (grise) | Grossière et hyperchromatique, parfois finement granulaire, répartition homogène |
| Nucléoles | Isolés à multiples, réguliers, non présents dans toutes les cellules | Nombreux, proéminents, lisses à irréguliers, isolés à multiples | Souvent présents, petits, parfois multiples |
Adénocarcinome endométrial
60x
Adénocarcinome endocervical
60x
SCC
60x
- DeMay RM: The Art & Science of Cytopathology. Chicago, IL. ASCP Press, 1996, pp 122-127.
- Guidos BJ et al: Detection of endometrial adenocarcinoma with the ThinPrep Pap test. Acta Cytol 1999; 43(5): 903.
- Johnson JE et al: Endocervical glandular neoplasia and its mimics in ThinPrep Pap tests. A descriptive study. Acta Cytol 1999;43(3):369-75.
- Papillo J et al: Increased specificity in the detection of glandular lesions: Decreased false positive AGUS with ThinPrep Pap tests. Acta Cytol 1999; 43(5): 902.
- Tao L-C: Cytopathology of the Endometrium Direct Intrauterine Sampling. Chicago, IL. ASCP Press, 1993, pp 71-107.