Gyn Atlas Abschnitt 1
DANKSAGUNG
Suzanne M. Werneke, BA, CT(ASCP)
Unser Dank gilt Kurt Douglass, CT(ASCP) für seine Bemühungen, dieses Projekt zu vollenden und für die ursprüngliche Version des ThinPrep® Morphology Reference Manuals, welches weiterhin in Gebrauch ist. Dank gilt ebenfalls Mike LeDonne, CT(ASCP) für viele seiner frühen Digitalfotos, die in diesem Atlas Verwendung finden.
Ich möchte persönlich allen unseren Gastautoren danken, die hart gearbeitet haben um unsere Zeitlimits einzuhalten. Wir haben viel von jedem dieser Pathologen und ZTAs gelernt, deren Enthusiasmus wir so sehr schätzen und deren Begeisterung für die Zytologie wir bewundern.
Schließlich vielen Dank an Charlotte L. Brahm, CT(ASCP), die verantwortliche Redakteurin, deren Name an keiner Stelle in diesem Atlas auftaucht, die aber unermüdlich arbeitete um sein Gelingen zu ermöglichen.
Mitarbeiter:
Raheela Ashfaq, MD
Professor, Department of Pathology, University of Texas Southwestern Medical Center, and Director of Cytopathology and Oncodiagnostic Laboratory, Parkland Health and Hospital, Dallas, TX
R. Marshall Austin, MD, PhD
Medical Director and Director of Cytopathology and Gynecologic Pathology Services, Coastal Pathology Associates, Charleston, SC
John M. Bauer, MD
Medical Director, Piedmont Pathology, Incorporated, Hickory, NC
Diane D. Davey, MD
Professor of Pathology and Laboratory Medicine, Director of Cytopathology and Bone Marrow Service, Director of Cytopathology Fellowship Program, University of Kentucky, Lexington, KY
Luis A. Diaz-Rosario, MD
Medical Director, Anatomic Pathology, Quest Diagnostics, Incorporated, Tampa, FL
Martha L. Hutchinson, MD, PhD
Associate Professor Pathology, Brown University, Providence, RI
Deanna K. Iverson, MHS, SCT(ASCP), HTL
Pathology Manager, Palo Alto Medical Foundation, Palo Alto, CA
Joyce E. Johnson, MD
Associate Professor, Department of Pathology, Director Division of Education, Vanderbilt University Medical Center, Nashville, TN
James Linder, MD
Medical Director, Hologic, Inc., Marlborough, MA; Professor, Pathology and Microbiology,
University of Nebraska Medical Center, Omaha, NE
Jacalyn L. Papillo, BS, CT(ASCP)
Cytopathology Manager, Fletcher Allen Healthcare, Burlington, VT
Pamela Smith Piraino, CT(ASCP)
Clear Path Diagnostics, Syracuse, NY
Richard A. Smith, MD, PhD
Chief of Pathology, Sturdy Memorial Hospital, Attleboro, MA
Zahniser, David, PhD
President, Diagnostic Vision Incorporated, Wellesley, MA
EINFÜHRUNG
Dieser Atlas wurde geschrieben um Zytologieassistenten/innen, Zytologen und Pathologen zu helfen, ihre Fähigkeiten in der Interpretation von Präparaten der gynäkologischen Zytologie mit dem ThinPrep® Pap Test zu entwickeln und zu vertiefen. Die frühe Forschung und die Entwicklung des ThinPrep® Pap Tests durch die Firma Hologic schufen die Grundlagen für die Vergleiche mit dem konventionellen Pap-Abstrich. Seither haben Zytologieassistenten/innen und Pathologen in der Praxis weltweit mitgeholfen, diese Basis zu verfeinern. Dieser Bildatlas soll als Ausbildungsmittel und als fortdauernde Referenz für Nutzer des ThinPrep® Pap Tests dienen.
Der Aufbau des Atlas entspricht dem Bethesda-System, wie es im National Cancer Institute entwickelt und in einer Publikation von Robert J. Kurman und Diane Solomon, unter dem Titel “The Bethesda System for Reporting Cervical/Vaginal Cytologic Diagnoses: Definitions, Criteria and Explanatory Notes for Terminology and Specimen Adequacy” (New York: Springer-Verlag, 1994) zusammengefasst wurde. Updates mit der Bethesda 2001 Nomenklatur wurden eingeschlossen. Das Buch “The Art and Science of Cytopathology” von Dr. Richard DeMay wurde zur Definition zytologischer Kriterien bezüglich Atypie, Dysplasie und höhergradiger Läsionen benutzt.
Zur Erleichterung der Nutzung in Deutschland und der Schweiz wurde in den Anhang eine Tabelle eingefügt, welche die jeweilige Kategorie des Bethesda-Systems mit den länderspezifischen Kategorien der zytologischen Nomenklatur korreliert.
Für jede diagnostische Kategorie illustrieren Bilder die ThinPrep® Pap Test (TPPT)-Morphologie, das korrespondierende Bild des konventionellen Pap-Abstriches und die entscheidenden Look-Alikes. Alle Fotografien in diesem Atlas bilden, falls nicht anders angegeben, ThinPrep® – Präparate ab. Diese Fotografien sollen typische Befunde auf den ThinPrep® -Präparaten illustrieren. Sie können einer individuellen Interpretation unterworfen sein.
ÜBERBLICK ÜBER DAS
THINPREP®-PRÄPARATIONSVERFAHREN
Das TP-System für Pap-Abstriche ist von der US-amerikanischen Arzneimittelbehörde FDA als Ersatz der konventionellen Methode, atypische Zellen, das Zervixkarzinom und seine Vorstufen und andere zytologische Kategorien wie sie im Bethesda-System definiert werden zu entdecken, zugelassen. Es ist nachgewiesen, dass der TPPT signifikant effektiver als der konventionelle Pap-Abstrich ist, niedriggradige intraepitheliale Läsionen (LSIL) und schwerere Läsionen in einer Vielzahl verschiedener Patientenpopulationen zu entdecken. In einer direct-to-vial-HSIL-Studie fand sich eine Steigerung des Nachweises von HSIL um 59,7%. Die Präparatequalität ist ebenfalls gegenüber dem konventionellen Pap-Abstrich signifikant verbessert.
Optimale Probenentnahme und Präparation sind die wichtigsten Faktoren bei der Verbesserung der Genauigkeit des Pap-Tests. Unterschiede in den Verfahren, konventionelle Pap-Abstriche und TPPT-Proben aufzubereiten führen zu Unterschieden im mikroskopischen Erscheinungsbild zwischen konventionellen und TP-Abstrichen. Eine korrekte Interpretation von TPPT-Präparaten setzt die Kenntnis des TP-Präparationsverfahrens voraus. Dies ist besonders wichtig im Hinblick auf die Qualitäten des Abstrichs, welche die Erhaltung und Präsentation des Präparates beeinflussen. Daher wird das TP-Präparationsverfahren im Folgenden zusammenfassend beschrieben.
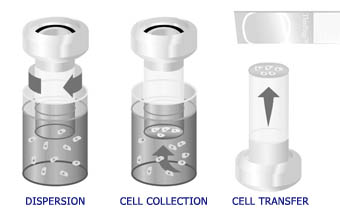
Der automatisierte Vorgang im ThinPrep® -Prozessor umfasst eine Aufschüttelung der Probe, eine Präzisionsfiltration um Zellen auf eine Membran aufbringen und den Transfer auf einen Objektträger.
TP-Prozessor:
Funktionsprinzipien
Der TP-Prozess beginnt mit der Entnahme des gynäkologischen Abstrichs der Patientin durch den Arzt entweder mit einem besenartigen Instrument oder einer Kombination aus Bürste und Plastikspatel. Das Abstrichinstrument wird dann im Probengefäß, welches die PreservCyt® – Lösung enthält, ausgespült. Die TP-Probe wird nun verschlossen, beschriftet und in ein Labor geschickt, das mit einem TP-Prozessor ausgerüstet ist.
Im Labor wird das Probengefäß mit dem zugehörigen Zytologieanforderungsschein abgeglichen und eine Zytologienummer wird für das Formular, das Gefäß und einen Objektträger vergeben. Gefäß und zugehöriger Objektträger werden zusammen mit einem Gynäkologie-Einmalfilterzylinder (durchsichtiger Filter) in den TP-Prozessor eingesetzt und der Bediener wählt den entsprechenden Bearbeitungsmodus. Das Gerät homogenisiert die Probe indem es entweder den Filter (T2000) oder das Probengefäß (T3000) rotiert und damit in der Flüssigkeit Scherkräfte generiert, die stark genug sind, zufällig adhärentes Material zu trennen, Blut, Schleim und zur Diagnosestellung irrelevanten Debris aufzulockern, während echte Zellverbände intakt bleiben. Wenn das Abnahmeinstrument hinreichend ausgespült wurde, gelangen alle entnommenen Zellen in die Lösung anstatt am Instrument zu verbleiben und weggeworfen zu werden wie beim konventionellen Pap-Abstrich. Diese Tatsache zusammen mit der Randomisierung der Probe während der Rotationsphase ermöglicht den Transfer einer repräsentativen Zellprobe auf den Objektträger und eine exaktere Begutachtung des zytologischen Status der Patientin.
Anschließend werden die Zellen durch Applikation eines leichten Vakuums, welches Flüssigkeit durchsaugt, auf die Membran des TransCyt-Filters aufgebracht. Wenn das Probenmaterial sich auf der Filtermembran sammelt, werden die Poren der Membran besetzt und damit der Prozessor veranlasst, die Aspiration zu beenden. Die Flußrate durch den TransCyt-Filter wird ständig kontrolliert um die Variabilität der Präparate zu minimieren.
Wenn der Prozessor den Filtrationsschritt beendet, wird der Filterzylinder aus dem Probengefäß zurückgezogen und gekippt, um das Filtrat in den Abfallbehälter zu entleeren. Der Filterzylinder wird dann zum Objektträger gedreht. Mit einem Druckluftsystem werden die Zellen vom Filter auf den Objektträger übertragen. Aufgrund der natürlichen Adhäsionseigenschaften von Zellen und der elektrochemischen Eigenschaften der TP- Objektträger haben die Zellen eine höhere Affinität zum Objektträger als zum Filter und eine dünne Zellschicht von 20 mm Durchmesser wird auf den Objektträger transferiert. Wenn der Zelltransfer vollständig durchgeführt wurde wird der Objektträger vom Filterzylinder entfernt und automatisch in ein Fixierungsbad gegeben. Er wird dann vom Bediener entnommen und zur folgenden Routine-Papanicolaoufärbung und Eindeckung in ein Färberack (T2000) eingesetzt. Beim T3000-Prozessor wird der Objektträger im Gerät sprayfixiert und für die folgende Routinefärbung und Eindeckung in ein Färberack eingesetzt.
Quellenangaben:
- Hutchinson ML, et al: Homogeneous sampling accounts for the increased diagnostic accuracy using the ThinPrep® Processor. Am J of Clin Pathol 1994; 101:215-219.
- ThinPrep® 2000 System Package Insert, Hologic, Inc., 2001.
- TP® 2000 Operator’s Manual, Rev G, Hologic, Inc., 2000.
- TP® 3000 Operator’s Manual, Rev C, Hologic, Inc., 2000-2001.
Wissenschaftliche Grundlagen
David Zahniser, PhD
Der falsch-negative Pap-Abstrich ist ein entscheidendes Qualitätsproblem für das zytologische Labor. Das Unvermögen, Zervixneoplasien zu entdecken, beruht entweder auf Entnahme- oder Screeningfehlern. Für die Mehrheit falschnegativer Pap-Abstriche, insgesamt etwa 60-80% der Fälle, sind Entnahmefehler verantwortlich. Screening- und Interpretationsfehler machen den Rest aus. Ursprünglich wurden Abnahmefehler dem Kliniker angelastet, der die Läsion bei der Zellentnahme nicht richtig abgestrichen habe. Man war der Annahme, dass die Läsion entweder zu klein war oder sich zu hoch im Zervikalkanal befand. Es hat sich herausgestellt, dass Entnahmefehler eine große Rolle für die Grenzen der Sensitivität des Pap-Tests spielen. Frühe Arbeiten bei der Entwicklung des ThinPrep®2000-Systems halfen, inhärente Probleme bei der Aufbereitung des konventionellen Pap-Abstrichs aufzudecken und definierten Entnahmefehler besser. Studien haben mittlerweile gezeigt, daß Entnahmefehler nicht notwendigerweise vom Arzt abhängen, sondern spezifisch mit Limitationen der konventionellen Abstrichtechnik verbunden sind.
Die Ursprünge der ThinPrep®-Technologie gehen zurück in eine Zeit, als in der Forschung verschiedene Anstrengungen unternommen wurden, ein quantitatives System zur Analyse von Pap-Abstrichen zu entwickeln. In den 60-er Jahren machten es die ersten Computer möglich, Bilderfassungssysteme zu entwickeln. Von Anfang an waren Computerbilderfassungssysteme durch ungleichmäßige konventionelle Abstriche limitiert. Es war offensichtlich, dass traditionelle Zervixabstriche für eine Analyse durch ein automatisches System zu kompliziert waren. Mit hohem Forschungsaufwand bemühte man sich, Geräte für maschinenlesbare Präparationen zu entwickeln. Automatisierte Präparationssysteme der ersten Generation wurden entwickelt um eine Einzelzellpopulation ohne Zellgruppen zu erreichen, welche einer Analyse durch die damaligen primitiven Computer zugänglich sein sollte. Um diese Zelllagen und -gruppen aufzulösen, wurden verschiedene mechanische Mittel getestet. In Lösung eingebrachte Zervixabstriche wurden heftigen mechanischen Belastungen ausgesetzt. Die erfolgreichsten Präparationsvorrichtungen benutzten Spritzensysteme, welche die Zellprobe durch eine großkalibrige Kanüle pumpten um eine Einzelzellpopulation zu erhalten. Diese Geräte waren in der Lage, dem Computer eine vereinfachte Zellpopulation zu präsentieren. Leider war eine erfolgreiche Zellvereinzelung mit Zellverlust verbunden und die Gewebearchitektur wurde bei dem Prozess zerstört. Damit wurde natürlich die weitere Begutachtung beeinträchtigt. Arbeiten in den Niederlanden befassten sich mit einigen der Probleme, welche bei der Aufbereitung mit Spritzen auftraten. Sie gingen den Dispersionsschritt mit der Verwendung eines Zylinders an, der sich mit hoher Geschwindigkeit in der Zellsuspension drehte. Die Überlegung war, mit dem rotierenden Zylinder Schwerkräfte, ähnlich wie bei der Spritzenaufarbeitung, zu generieren. Über die Kontrolle der Geschwindigkeit der Zylinderrotation konnte der Grad der Vereinzelung beeinflusst werden. Die gegenwärtigen ThinPrep®-Prozessoren verwenden die Zylinderdispersionstechnik indem sie eine viel niedrigere Dispersionsgeschwindigkeit einsetzen um die Integrität der natürlichen Zellbindungen zu erhalten. Zusätzlich wurde die Zellaufnahmeflüssigkeit modifiziert um die Probenpräparation weiter zu optimieren.
Ein Filtrationsverfahren in Verbindung mit dem Dispersionsschritt war ebenfalls in der Entwicklung. Die Qualität der Probe konnte durch Verringerung unspezifischer Hintergrundelemente weiter verbessert werden. Sorgfältig wurde darauf geachtet, keine wesentliche diagnostische Information, die ursprünglich in der Probe enthalten war, zu verlieren. Eine Plastikfiltermembran wurde eingesetzt um das Zellmaterial aus der Flüssiglösung zu konzentrieren und so Artefakte wie sie bei einer einfachen Filtration auftreten können, zu vermeiden. Der Herstellungsprozess dieser Filter resultiert in einer gleichmäßigen Verteilung von Poren einheitlicher Größe.
Das Aufbereitungsgerät benötigte einen zusätzlichen Schritt, die Zellen aus der Suspension auf einen Objektträger zu bringen. Zahlreiche Techniken wurden untersucht um die Auftragung der Zellen so zu optimieren, damit sie sowohl für eine menschliche als auch für eine Computeranalyse geeignet sind. Die Benutzung der Filtermembran erlaubte den Zelltransfer durch Anpressen des Filters mit den Zellen an den Objektträger, was zu einer dünnen, gleichmäßigen Zelllage mit einheitlicher Verteilung und unveränderter Zellmorphologie führt.
Mangel an Zytologieassistenten/innen und forensische Probleme haben das Interesse an einer Automatisierung des Pap-Abstrichs wieder aufleben lassen. Zahlreiche Computerscreening-Geräte sind auf dem Markt. Trotz der Fortschritte in der Computertechnologie bleibt die gleichmäßige Präparation des Abstrichs eine Notwendigkeit. Die ThinPrep®-Technologie hat Bedeutung gewonnen, die Limitationen der Präparation zu überwinden und nichtklinische und klinische Studien, welche die ThinPrep-Technologie unterstützen, haben dazu beigetragen, die Grenzen des Pap-Abstrichs besser zu verstehen.
Quellenangaben:
- Linder J and Zahniser: ThinPrep Papanicolaou testing to reduce false-negative cervical
MIKROSKOPISCHE BEGUTACHTUNG VON THINPREP® ABSTRICHEN
Deanna K. Iverson, MHS, SCT(ASCP), HTL
George Papanicolaou entwickelte die morphologischen Kriterien des konventionellen Pap-Abstrichs in den frühen 20-er Jahren. Mit der Zeit wurden aufgrund zahlreicher Studien Modifikationen eingefügt, welche gut dokumentiert sind. Es bestehen geringe Unterschiede zwischen den grundlegenden morphologischen Kriterien des traditionellen Abstrichs und des ThinPrep® PapTests. Die einzigen mikroskopischen Unterschiede sind im Allgemeinen mit der Flüssigkeitssammelmethode des ThinPrep® Systems verbunden. Es ist wichtig anzumerken, dass die Gewebearchitektur bei der maschinellen Aufbereitung nicht verändert und dass die klassische Zellmorphologie für die Beurteilung verwendet wird. Die morphologischen Ähnlichkeiten zwischen dem ThinPrep® und dem konventionellen Pap-Abstrich überwiegen bei weitem die Unterschiede und Erfahrungen mit der konventionellen Morphologie sind leicht zu transferieren. Das folgende Kapitel ist eine Zusammenfassung von Schlüsselmerkmalen der morphologischen Charakteristika des ThinPrep® -PapTests und eine Anleitung zum Screenen um Auffälligkeiten möglichst gut zu entdecken.
Wie beim konventionellen Pap-Test sollte das Screenen von ThinPrep® PapTest-Abstrichen durch ein langsames, systematisches Betrachten überlappender Felder erfolgen. Der runde Rand des Zellbelags auf dem ThinPrep®-Präparat kann als Referenzpunkt benutzt werden. Vor der systematischen Beurteilung des Abstrichs bei geringer Vergrößerung (10x) kann es sinnvoll sein, das Präparat einmal rasch mit der Übersichtsvergrößerung durchzusehen, um die zelluläre Zusammensetzung und das Vorhandensein von Endozervikalzellen zu beurteilen und die technische Qualität des Abstrichs zu prüfen.
Erfahrene Zytologieassistenten/innen, Pathologen und Zytologen können die verschiedenen Zelltypen auf ThinPrep® Pap-Abstrichen leicht identifizieren. Der Zytologe wird weiterhin Fällen begegnen, die komplex sind und einer sorgfältigen Untersuchung bedürfen. Quantitative Bewertungen der Zellularität (normale und auffällige Populationen) können ähnlich wie bei der konventionellen Zytologie weiter vorgenommen werden. Jedoch ist bei ThinPrep® Pap-Abstrichen die Anzahl auffälliger Zellen weniger entscheidend als ihr eindeutiges Vorhandensein oder ihr Fehlen.
Die einzigartigen Charakteristika des ThinPrep® PapTests umfassen die Gleichmäßigkeit der Zellpräparation, die Flüssigfixierung, die Zellgröße, das Abstrichmuster und den Präparatehintergrund.
Gleichmäßigkeit der Zellpräparation:
- Konzentriert
- Gleichmäßig verteilt
- 20mm Kreis
Da das Zellmaterial in der Lösung aufgenommen und dann gefiltert wurde, erscheint die Darstellung des Präparates auf dem ThinPrep® Pap Test-Abstrich manchmal etwas anders als auf konventionellen Pap-Abstrichen. Dieser weist dichte und weniger dichte Bereiche auf, hat Lufttrocknungsartefakte und häufig ist das Zellmaterial mechanisch alteriert. Das Zellmaterial auf dem ThinPrep® PapTest-Abstrich ist konzentriert und gleichmäßig auf einen 20 mm messenden Kreis verteilt. Epithellzelllagen kommen weiterhin zur Darstellung aber es gibt weniger Zellüberlagerungen.
Flüssigfixierung:
- Zellen runden sich in Lösung ab
- Verbesserte Darstellung zytoplasmatischer Details
- Fixierungslösung auf Methanolbasis
- Verbesserte Darstellung von Kerndetails
- Variabilität der Kernfärbeintensität
Flüssigkeitsfixierung: Was den ThinPrep® Pap Test einzigartig macht, ist die Aufnahme des Zellmaterials in einer Flüssigfixierungslösung. Die Zellmorphologie von ThinPrep® Pap Test-Abstrichen ist ähnlich der von nicht-gynäkologischen Abstrichen, was sich darin zeigt, dass die Zellen dazu tendieren, sich in der Lösung abzurunden, jedoch sind die verschiedenen Zelltypen in ThinPrep® Pap Test-Abstrichen weiterhin leicht zu unterscheiden. Endozervikalzellen können stärker dreidimensional wirken und mit Endometriumzellen verwechselt werden. Die Palisadenstellung endozervikaler Zellen kann bei starker Vergrößerung häufig in der Peripherie von Zellverbänden gesehen werden.
Die Fixierungslösung des ThinPrep® Pap Test-Abstrichs enthält Methanol, was die Konservierung von Zellstrukturen und Kernmorphologie fördert. Die verbesserte Erhaltung zytoplasmatischer Details lässt Herkunft und Reifestadium von Zellen besser bestimmen. Die bessere Konservierung der Kernmorphologie ist primär das Ergebnis der Flüssigfixierung. Kerne können überinterpretiert werden. Daher ist bei der Bewertung von ThinPrep® Pap Test-Abstrichen Zurückhaltung angebracht, um eine Überinterpretation von gut konservierten Kernen zu vermeiden. Die Betonung von Kernstrukturen bei ThinPrep® Pap Test-Abstrichen ist ähnlich jener, die bei konventionellen Pap-Abstrichen auftritt, welche mit 95%igem Ethanol fixiert wurden.
Die nukleäre Hyperchromasie, welche typischerweise auf konventionellen Pap-Abstrichen mit plattenepithelialen Läsionen assoziiert ist, kann auf ThinPrep® Pap Test-Abstrichen reduziert sein. Aus diesem Grund kann die diagnostische Aussagekraft einer Hyperchromasie auf ThinPrep® Pap Test-Abstrichen begrenzt sein. Falls Hyperchromasie vorliegt, sollte sie in die Bewertung des Abstrichs mit eingehen, aber ihr Fehlen sollte nicht dazu führen, dass Kernatypien unbeachtet bleiben. Beim Fehlen einer Hyperchromasie kann die exakte Interpretation von hochgradigen Läsionen auf ThinPrep® Pap Test-Abstrichen eine besondere Herausforderung sein, da man sich auf Veränderungen in Kerngröße und -form verlassen muss – morphologische Kriterien, welche beim konventionellen Pap-Abstrich häufig übersehen oder nicht in die Bewertung einbezogen werden.
Zellgröße:
- Proportional kleiner
- Einzelzellen prominenter
Zellgröße: Aufgrund der Flüssigfixierung können die Zellen von ThinPrep® Pap Test-Abstrichen proportional kleiner erscheinen. Eine gut erhaltene Intermediärzelle ist eine nützliche Referenz bei der Bestimmung von Zell- und Kerngröße. Dies ist besonders wichtig bei der Beurteilung und Einstufung von kleinen, unreifen Zellen metaplastischen Typs. Es ist wichtig, diese Zellen bei starker Vergrößerung zu betrachten um, besonders beim Fehlen einer Hyperchromasie, den Kern sorgfältig auf Atypien zu untersuchen.
Einzelzellen sind verteilt und erscheinen beim ThinPrep® System charakteristischerweise als Teil einer „randomisierten Subpopulation“. Da Blut- und Entzündungszellen diese Zellen nicht verdecken, entsteht der Eindruck, es gäbe mehr Einzelzellen als beim konventionellen Pap-Abstrich.
Abstrichmuster:
- „Ausstrich“-Muster eliminiert
- Hintergrundmuster verändert
Abstrichmuster: Im Allgemeinen sind Zellarchitektur und Hintergrund auf ThinPrep® Pap Test-Abstrichen ähnlich dem, was man auf gut erhaltenen konventionellen Pap-Abstrichen sieht. Das Zellmaterial auf ThinPrep® Pap Test-Abstrichen ist gleichmäßig und einheitlich verteilt. Die Gewebearchitektur ist erhalten (Sheets und Synzytien) und mechanische Alterationen sind signifikant reduziert.
Hintergrund: Anders als bei konventionellen Pap-Abstrichen ist der Hintergrund von ThinPrep® Pap Test-Abstrichen im Allgemeinen sauber. Daher fällt es leichter, normale und auffällige Zellpopulationen zu identifizieren. Blut, Schleim, Entzündungselemente und Tumordiathese sind auf dem ThinPrep®-Abstrich vorhanden, aber wegen der Unterschiede in der Zellentnahme und -aufbereitung stellen sie sich etwas anders dar als auf dem konventionellen Pap-Abstrich. Die Anwesenheit von Blut oder Entzündungszellen auf ThinPrep® Pap Test-Abstrichen überdeckt selten das Präparat, wenn sie nicht das wesentliche Material sind, welches beim Pap-Abstrich erhalten wurde. Frisches Blut wird von dem hämolytischen Reagenz im Flüssigmedium aufgelöst. Dies führt dazu, dass die Erythrozyten farblos erscheinen („Geisterzellen“). Altes Blut wird nicht völlig lysiert und führt zu einer Rotfärbung verschiedener Intensitität. Die Fähigkeit, frisches von altem Blut zu unterscheiden, kann bei der Diagnose maligner Veränderungen nützlich sein.
Entzündliches Material wird auf den ThinPrep® Pap Test-Abstrichen noch gleichmäßiger verteilt. Es kann häufig an epithelialen Zellen adhärent sein. Gelegentlich kann der Hintergrund „dreckig“ wirken. Das Material auf dem Abstrich erscheint schmutzig und zerfetzt und es gibt nur wenige gut erhaltene Plattenepithelien. Wenn ein solcher Hintergrund gesehen wird, ist es wichtig, an Folgendes zu denken: Vorhandensein eines infektiösen Agens, Zytolyse und/oder eine maligne Läsion (Tumordiathese). Falls vorhanden, kann eine Tumordiathese (Entzündungszellen, Erythrozyten, Fibrin, nekrotischer Zelldebris und granuläre Eiweißpräzipitate) auf ThinPrep® Pap Test-Abstrichen durch den Hintergrund der Präparation hindurch wahrgenommen werden. Die epithelialen Zellen werden umgeben oder überlagert (“clinging” diathesis).