PLATTENEPITHEL
PLATTENEPITHEL
AUFFÄLLIGE PLATTENEPITHELIEN
Richard A. Smith, MD, PhD
Keine diagnostische Einstufung löst mehr Diskussionen aus als die der atypischen Plattenepithelzellen (ASC). Die revidierte Klassifikation des Bethesda-Systems (TBS) 2001 hat neue Termini geschaffen. Das TBS sagt aus, dass die ASC-Kategorie in Betracht gezogen werden sollte, wenn Auffälligkeiten des Plattenepithels vorliegen, die ausgeprägter sind als jene, welche reaktiven Veränderungen zugeordnet werden, aber qualitativ oder quantitativ nicht die diagnostischen Kriterien für eine niedriggradige oder hochgradige intraepitheliale Läsion erfüllen. Weiterhin legt das TBS Wert darauf, diese Diagnose als „unklare Ätiologie“ (ASC-US) oder als „HSIL kann nicht ausgeschlossen werden“ (ASC-H) einzustufen.
Die richtige Einstufung von ASC ist eine Herausforderung für Zytologieassistenten/innen, Zytologen und Pathologen. Ein Kapitel über die morphologischen Kriterien von ASC zu schreiben ist in Anbetracht der Subjektivität dieser Interpretation ebenfalls eine schwierige Aufgabe. Seit der Einführung des TBS haben Zytologen bei der Bewertung des konventionellen Pap-Abstrichs diese Kategorie als ein “Sammelbecken” für Abstriche benutzt, die schwierig einzustufen sind.
Die dem konventionellen Pap-Abstrich eigenen Artefakte, wie Luftrocknung oder partiell überlagerte Zellen, können zu einer ASC-Diagnose führen. Der Grad der in reaktiven Zellen vorhandenen Atypie mag ebenfalls durch Lufttrocknung oder Ausstreichen überzeichnet werden. Diese Probleme führen zu Artefakten, welche es Zytoassistenten/innen, Zytologen und Pathologen schwer machen, die Kerndetails der fraglichen Zellen adäquat zu sehen, was zu einer unklaren Diagnosestellung führt
Die sofortige Nassfixierung des ThinPrep®-Verfahrens kann es dem/der Zytologieassistenten/in, dem Zytologen oder Pathologen erlauben, sich von dem „ASC-Sammelbecken“ zu verabschieden und besser zwischen reaktiven Veränderungen, eindeutiger plattenepithelialer Atypie und Dysplasien zu unterscheiden. Dies bedeutet nicht, dass ASC-Bewertungen durch die Einführung des ThinPrep® PapTests eliminiert werden, aber das Laborpersonal hat die Möglichkeit, seine morphologischen Kriterien zu verfeinern und damit bestimmte ASC-Fälle zu eliminieren, deren Ursache in einer unzureichenden Aufbereitung liegt, und die Fälle besser zu erfassen, die Auffälligkeiten beinhalten.
Der ThinPrep® PapTest minimiert die problemträchtigen Artefakte, welche dem Ausstrichpräparat und der Sprayfixierung inhärent sind. Dies erlaubt eine adäquate Betrachtung des Kerns, was die Findung einer definitiven Diagnose anhaften. Die Epithelzellen die in die ASC-Kategorie eingestuft werden, sind meistens reife Plattenepithelien und Metaplasien, die minimale Veränderungen aufweisen, welche für eine LSIL- oder HSIL-Diagnose nicht ausreichen. Die Kerne sind leicht vergrößert und diese Vergrößerung bezieht sich auf die normalen Vertreter des gleichen Zelltyps. Die Kerne können leichte Unregelmäßigkeiten der Kernmembran aufweisen, diese sind aber meist glatt. Wenn es sich um Metaplasiezellen handelt, muss man darauf achten, dass die Unregelmäßigkeiten nicht darauf zurückzuführen sind, dass eine Vakuole(n) den Kern in eine abweichende Form drückt. Das Chromatinmuster ist fein granulär und gleichmäßig verteilt. Chromozentren oder Nukleoli sind meist unverdächtig oder fehlen, außer/es sei denn eine reaktive Veränderung tritt zusammen mit der Atypie auf. Hier muss die Differentialdiagnose einer reaktiven Veränderung unter dem Aspekt des Vorkommens oder des Fehlens der anderen Kriterien neu geprüft werden.
Bei konventionellen wie bei ThinPrep®-Abstrichen kann eine ASC-Interpretation aus jeder von mehreren unterschiedlichen zellulären Veränderungen hervorgehen. Dazu gehören u. a. plattenepitheliale Zellveränderungen, die atypische Metaplasie und atypische Parakeratose. Nachfolgend die Kriterien für ACS im ThinPrep® PapTest sind die Folgenden:
LOOK-ALIKE:
| REAKTIV | ASC-US | LSIL | |
| Kern | 1,5-2x vergrößert, flach | 2 -3x vergrößert, flach bis minimale Raumtiefe | 3-4x vergrößert, geringe Raumtiefe |
| Kernmembran | Glatt | Glatt bis leicht irregulär | Glatt bis leicht irregulär |
| Chromatin | Feinkörnig, gleichmäßig verteilt | Feinkörnig, gleichmäßig verteilt | Etwas grobkörniger, gleichmäßig verteilt |
| Nukleoli/Chromozentren | Klein bis auffällig, manchmal multipel | Auffällig oder fehlend | Fehlend |
| Zytoplasmatische Merkmale | Perinukleäre Halos | Fragliche Vakuolen | Diagnostische HPV-Vakuolen |
| Bichromasie | Kann vorhanden sein | Fehlend | Fehlend |
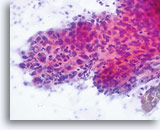
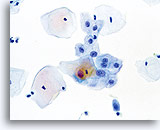
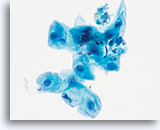
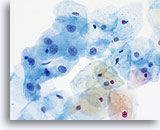
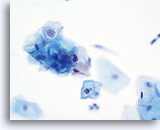
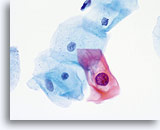
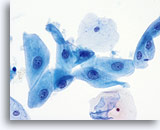
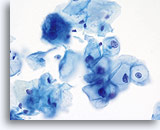
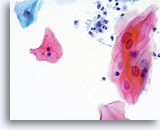
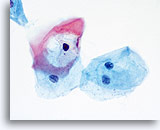
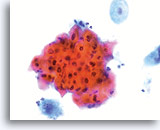
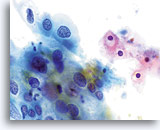
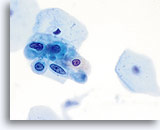
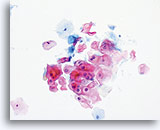
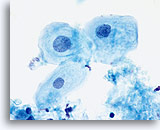
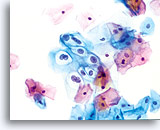
Die folgenden Bilder sind ThinPrep® Pap Test-Abstriche die am ehesten als reaktive Veränderungen, ASC-US und LSIL interpretiert werden können.
Wie bereits erwähnt, werden ASC-Befunde durch die Einführung des ThinPrep® Pap Tests nicht eliminiert. Die verbesserte Erhaltung der Zellen bei der Flüssigfixierung kann im Gegenteil sogar zur Überinterpretation von Kerngröße und Chromatin als ASC führen, wenn man nicht mit den im Kapitel „mikroskopische Beurteilung von ThinPrep®-Präparaten“ erörterten Folgen der Flüssigfixierung vertraut ist. Es kommt vor, dass das Laborpersonal direkt nach der Einführung des ThinPrep® Pap Tests vorübergehend eine Zunahme der ASC-Befunde bemerkt. Wenn dann erste Erfahrungen mit der neuen Methode gemacht wurden, sinkt die ASC-Rate unter jene beim konventionellen Pap-Abstrich.
Solange ASC eine Kategorie des TBS ist, wird es von Zytologen aufgrund der inhärenten Subjektivität der menschlichen Diagnosestellung und der variablen Interpretation diagnostischer Kriterien benutzt werden. Ebenfalls wesentlich ist in diesem Zusammenhang die Biologie humaner Papillomviren (HPV), welche morphologische Irritationen in Zellen verursachen, die geringgradiger sind als die einer LSIL. Die morphologischen Veränderungen, die durch HPV verursacht werden, werden detaillierter im Abschnitt über LSIL behandelt. Die Rolle dieser Viren bei der Entstehung von ASC hat die Möglichkeit geschaffen, das relative Risiko von ASC-Veränderungen durch sekundäre Testung von Hoch- vs. Niedrigrisiko-HPV-Typen aus dem ThinPrep® Pap Test-Gefäß zu bestimmen.
- Crum CP et al: Subclassifying atypical squamous cells in ThinPrep cervical cytology correlates with detection of high-risk human papillomavirus DNA. Am J Clin Pathol 1999; 112:384-90
- Dziura B et al: Improved ASCUS diagnosis: Clinical and financial implications for follow-up care. Ob, Gyn. News 1999; 1:12-13
- Ferenczy et al: Diagnostic performance of Hybrid Capture human papilloma virus deoxyribonucleic acid assay combined with liquid-based cytologic study. Am J Obstet Gynecol 1996;175(3 pt.1): 951-6.
- Ferris et al for the Atypical Squamous Cells of Undetermined Significance/Low-Grade Squamous Intraepithelial Lesions Triage Study (ALTS) group: Cervicography for triage of women with mildly abnormal cervical cytology results. Am J Obstet Gynecol 2001;185(4):939-43.
- Hong et al: Comparative analysis of a liquid based Pap test and concurrent HPV DNA assay of residual samples. ACTA Cytol 2002;46(5):828-34.
- Lin WM et al: Molecular Papanicolaou tests in the twenty-first century: Molecular analyses with fluid-based Papanicolaou technology. Am J Obstet Gynecol 2000; 39-45
- Manos MM et al: Identifying women with cervical neoplasia: Using human papillomavirus DNA testing for equivocal Papanicolaou results. JAMA 1999; 281:1605-10
- Papillo J et al: Evaluation of the ThinPrep Pap Test in clinical practice: a seven-month 16,314 case experience in northern Vermont. Acta Cytologica 1998; 42:204-208
- Quddus et al: Atypical squamous metaplastic cells: Reproducibility, outcome, and diagnostic features on ThinPrep Pap Test. Cancer (Cancer Pathol) 2001:93:16-22.
- Quddus et al: Utility of HPV DNA detection in thin-layer, liquid-based tests with atypical squamous metaplasia. ACTA Cytol 2002;46(5):808-12.
- Sherman et al: Cervical specimens collected in liquid buffer are suitable for both cytologic screening and ancillary human papillomavirus testing. Cancer 1997;81:89-97.
- Sherman et al: Performance of liquid based , thin-layer cervical cytology: Correlation with reference diagnosis and human papilloma virus testing. Mod Pathol 1998;11:837-843.
- Wright et al for the ASCCP-sponsored Consensus Conference: 2001 consensus guidelines for the management of women with cervical cytologic abnormalities. JAMA 2002;287(16):2120-29.